自2025年4月发布《减少临床前安全性研究中动物试验的路线图》以来,美国食品药品监督管理局(FDA)已成功启动了多项关键举措,以用更优的替代方法取代动物实验。2026年4月20日,FDA发布了后续报告《非临床研究中减少动物实验:第一年进展及未来方向》,总结了FDA在实施路线图方面的进展情况,并明确了下一步的行动方向。

1、主要成就总结
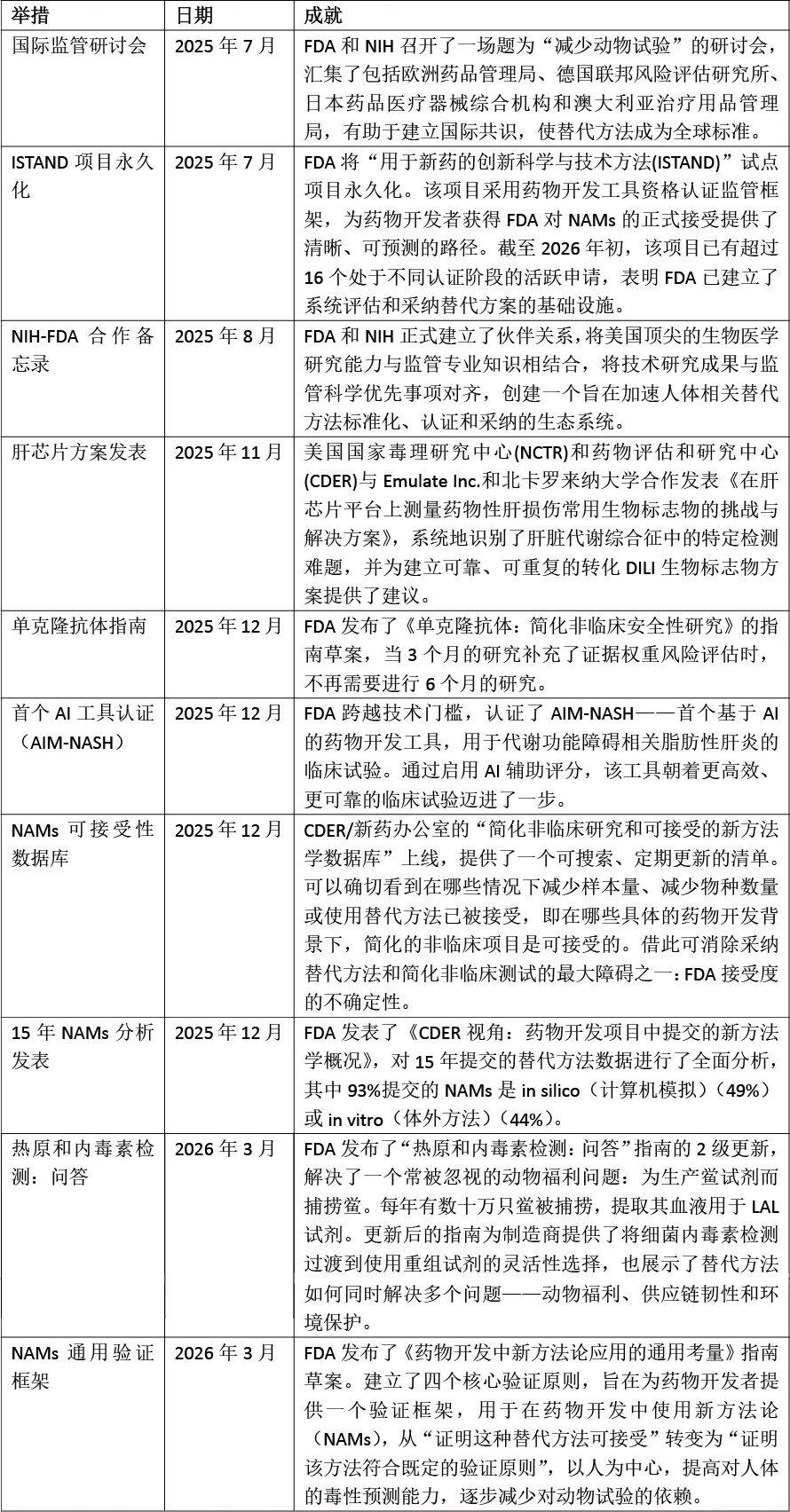
2、下一步行动方向
01 将减少测试时间范围扩展到单克隆抗体之外 单克隆抗体简化非临床研究的成功为其他药物类别提供了模型。FDA将把证据权重方法和减少测试时间的测试扩展到其他生物分子、新化学实体和医疗对策。虽然框架已经建立,但每一项扩展都需要仔细的科学评估以确保安全标准得以维持。 02 实施全面的指标和跟踪系统 为确保责任明确并衡量进展情况,FDA将采用系统来跟踪和量化药物开发项目中动物使用的变化。这些指标将使数据驱动的决策成为可能,以确定NAMs在哪些领域产生最大的效果,以及在哪些领域需要额外的指南或验证工作。 03 推进关键毒性终点的协调验证工作 基于15年分析显示93%的NAMs是in silico或in vitro方法,FDA将优先验证解决关键药物开发毒性终点的计算方法和体外方法,包括扩大器官芯片系统、计算毒理学模型和先进体外测试的验证。 04 建立毒性数据开放数据库 建立一个全面的国际毒性数据库,以便更好地利用现有数据并减少重复测试。目前在基础建设方面已取得进展,但全面实施需要继续开发数据库治理、数据标准化和国际数据共享协议。 05 覆盖所有关键终点的全面NAM工具箱 目前,某些毒性终点(皮肤致敏、致突变杂质)已有经过验证的替代方法,但其他毒性终点(发育毒性、慢性毒性)还没有。需要扩展系统的验证工作,以涵盖药物批准所需的全面安全性评估。 06 在证据权重框架中整合多种NAM 未来不是用单一替代方法替换每项动物研究,而是采用整合方法,其中多种NAM——计算模型、体外测试、器官芯片系统和人体数据——共同提供比任何单一方法更全面、更贴近人体的安全证据。 07 加强国际监管协调 随着替代方法变得更加复杂和依赖于具体场景,保持国际对齐变得更加重要,也更具挑战性。通过ICCVAM、ICH和双边监管合作持续参与将是必不可少的。 08 药物开发生态系统的文化转型 实现路线图愿景需要开发者(对提出替代方案有信心)、审评人员(评估新方法的专业知识)、研究人员(关注人体相关模型)和公众(理解替代方法可以提供更优安全证据)之间的文化变革与转型。
合律曼服务
✍️ QSAR建模服务 ✍️ QSAR软件服务 ✍️ COSMOS毒性预测 ✍️ 化妆品原料信息报送 ✍️ 化妆品注册备案
※ 版权声明:本文由合律曼数据整理,转载请注明出处!合律曼数据尊重知识产权,如内容涉及版权问题,烦请联系我们及时处理。合律曼数据随时为您更新化工新材料合规&数据跨境相关资讯,如有工业化学品REACH | 数据生产AI模型 | 数据标准与跨境交易 | 计算毒理QSAR | 全球SDS报告等相关问题欢迎咨询联系0571-86060701或点击下方图片在线咨询!
地址:浙江省杭州市拱墅区储鑫路21号网谷创新中心8幢903室
邮箱:info@compliancemen.com
QQ:3671987934

微信咨询

微信公众号
2012-2025 杭州合律曼数据服务有限公司版权所有 All Right Reserved 浙ICP备2025192110号-1 DESIGN BY WEETOP