
2026年2月,欧洲药品管理局(EMA)发布了《非诱变性杂质验证反思文件(Reflection paper on the qualification of non-mutagenic impurities)》(EMA/CHMP/4299/2026),为制药行业提供了一套替代传统动物试验的策略,用于评估药品中超过ICH Q3A/Q3B规定阈值的非诱变性杂质(NMIs)。这意味着,在杂质评估这一关键领域,监管机构正全速推动非动物测试方法的发展。而计算毒理学,在这场变革中扮演着不可替代的核心引擎角色。
1、文件核心目标与总体框架
文件明确指出,传统的使用“添加了杂质的原料药批次”进行动物实验的方法存在根本性局限:观察到的毒性很可能来自原料药而非杂质,因而难以得出杂质特异性的未观察到有害作用的水平(NOAEL)。更重要的是,当药品在有效期内的杂质水平发生变化时,动物试验往往需要重复进行,造成巨大资源浪费。这种做法也与欧盟第2010/63/EU号指令所倡导的3R原则(替代、减少、优化)相悖。
针对这一困境,文件提出了一个结构化的风险评估流程图(图1),展示了从最简捷路径到复杂路径的递进关系,在这一框架中,计算毒理学扮演着承上启下的关键角色——它不仅是独立的评估工具,也是支撑交叉参照(Read-across)、指导体外实验设计、以及最终进行证据权重分析的基础。
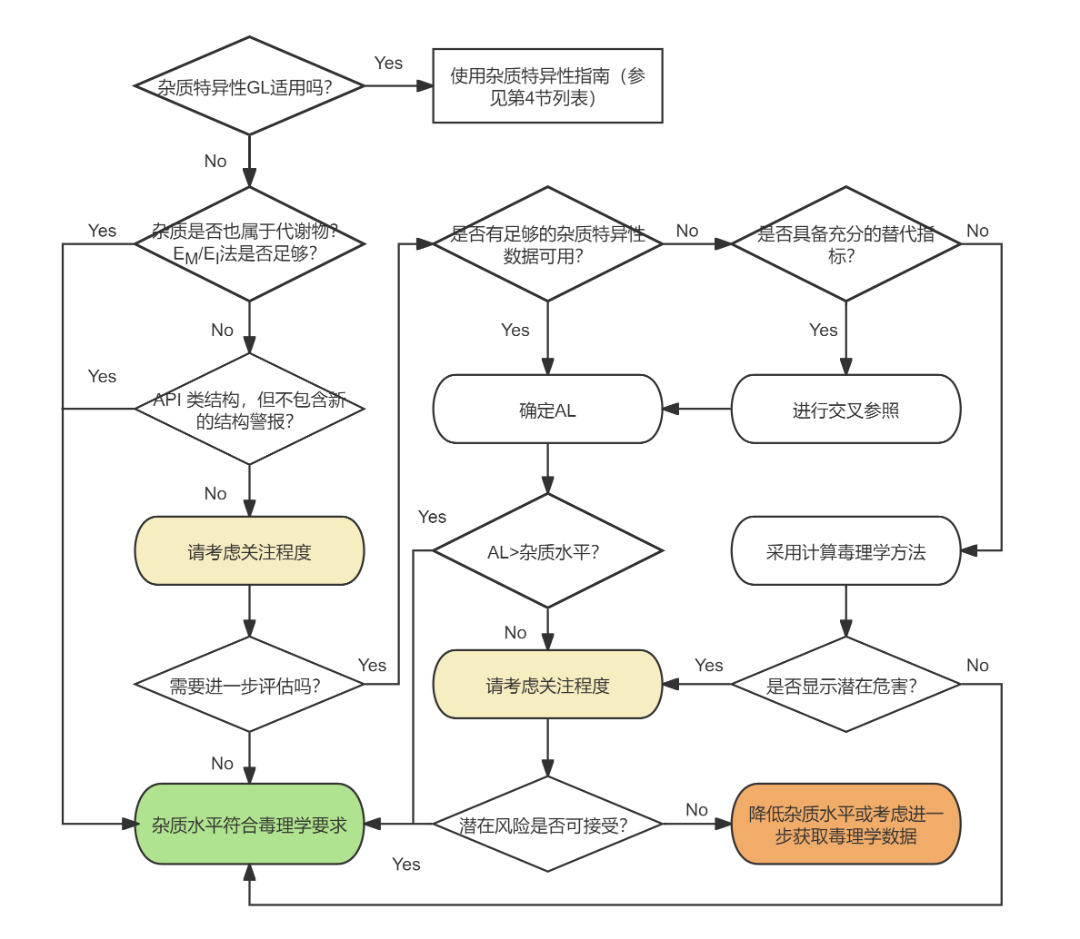
❅注:GL(Guideline)指指南,AL(Acceptable Level)指可接受水平
图1 非致突变性杂质的风险评估流程图
2、计算毒理学的核心地位与技术要求
文件对计算毒理学方法的应用提出了明确且严格的技术要求,这对于制药企业的合规实践具有重要指导意义。
文件强调,所使用的(定量)构效关系((Q)SAR)模型必须符合经济合作与发展组织(OECD)为监管目的制定的五项验证原则:
1) 明确的终点;
2) 明确的算法;
3) 明确的适用范围;
4) 良好的拟合度、稳健性和预测能力;5) 可能的机理解释。
计算工具应能预测对主要靶器官的潜在毒性,包括肝、肾、心血管、胃肠道、皮肤、中枢神经、呼吸系统,以及非诱变性致癌性。这意味着企业需要部署覆盖多毒性终点的预测能力体系。文件建议使用两种互补的方法进行预测,例如基于统计的QSAR模型和基于专家规则的模型,以增强预测结果的可信度。这一要求与ICH M7关于诱变性杂质评估的建议一脉相承,体现了监管机构对方法稳健性的重视。
3、新方法学的综合应用
文件不仅强调了计算毒理学的核心地位,还勾勒出一个整合多种新方法学(NAMs)的综合评估框架。
01 体外方法 (In vitro approaches)的靶向验证:
当计算毒理预测出潜在风险时,可以采用靶向的体外方法进行进一步验证或填补数据空白。
02 不良反应通路 (Adverse Outcome Pathways, AOPs)的整合应用:
可以整合来自计算毒理和体外研究的证据,通过AOP填补毒性事件的知识空白,为风险评估提供生物学上的合理性支持。
03 危害表征与证据权重:
目前NAMs主要用于危害识别,其用于定量风险评估的能力有限。但如果NAMs显示杂质对主要靶点没有危害,这一信息可以作为证据权重的一部分,支持杂质在特定水平下是安全的结论。这为企业提供了灵活而科学的论证路径。
4、对企业的启示:构建计算毒理学驱动的合规体系
面对EMA这份具有里程碑意义的指导文件,合律曼为制药企业提出以下战略建议:
#研发端:前置计算毒理学,实现杂质风险的早期识别
🔔核心建议:在工艺开发阶段即引入QSAR预测,从源头规避高风险杂质结构。
传统的杂质评估往往在工艺开发后期甚至临床阶段才启动,此时发现风险将面临高昂的工艺变更成本。企业应转变思路,在合成路线筛选和工艺设计阶段,就主动应用QSAR模型预测关键杂质(尤其是新出现的工艺杂质)的潜在靶器官毒性。
✅合律曼服务
合律曼提供的计算毒理学预测服务,能够基于分子结构快速评估杂质对肝脏、肾脏、心血管等主要靶器官的潜在风险,帮助企业:
◆ 对不可避免的杂质提前规划评估策略;
◆ 大幅降低后期因杂质问题导致的临床延误或注册风险。
#合规端:建立符合OECD标准的规范化评估流程
🔔核心建议:将QSAR/Read-across纳入杂质评估标准操作规程,确保合规证据的监管可接受性。
文件明确要求所使用的(Q)SAR模型必须符合OECD五项验证原则,这意味着简单套用公开模型或黑箱预测已无法满足监管要求。企业需建立或引入经过充分验证的、符合OECD标准的预测体系。
✅合律曼服务
合律曼依托专业计算毒理学团队,为企业提供:
◆ 符合OECD验证原则的QSAR预测报告:涵盖主要靶器官毒性及非诱变性致癌性等终点毒理信息;
◆ 专家驱动的Read-across论证:基于相似性原理,利用已知相似物的可靠数据填补评估缺口;
◆ 证据权重分析:整合计算预测、体外数据和AOP框架,构建科学完整的风险评估档案。
我们的报告体系严格遵循文件的技术要求,确保每一份预测结论都具备透明度、可追溯性和机理解释——这正是监管审评的核心关注点。、
以计算毒理学为引擎,赢取杂质评估新赛道
EMA这份反思文件的发布,标志着监管机构在杂质评估领域向非动物测试方法的重大转变。它不仅为行业提供了清晰的路线图和具体的技术要求,更传递出一个明确信号:以计算毒理学为核心的替代策略,已成为杂质安全性评估的必然选择。
※ 版权声明:本文由合律曼数据整理,转载请注明出处!合律曼数据尊重知识产权,如内容涉及版权问题,烦请联系我们及时处理。合律曼数据随时为您更新化工新材料合规&数据跨境相关资讯,如有工业化学品REACH | 数据生产AI模型 | 数据标准与跨境交易 | 计算毒理QSAR | 全球SDS报告等相关问题欢迎咨询联系0571-86060701或点击下方图片在线咨询!
地址:浙江省杭州市拱墅区储鑫路21号网谷创新中心8幢903室
邮箱:info@compliancemen.com
QQ:3671987934

微信咨询

微信公众号
2012-2025 杭州合律曼数据服务有限公司版权所有 All Right Reserved 浙ICP备2025192110号-1 DESIGN BY WEETOP